G蛋白偶联受体(GPCR)是人体最庞大的膜蛋白家族,负责无数化学信号传导,调控着视觉、嗅觉、心血管、免疫、神经和代谢等几乎所有核心生理过程。
据统计,FDA批准药物中高达35%直接靶向GPCR。
从治疗心衰的β受体阻滞剂,到过敏患者随身携带的抗组胺药,再到如今火爆的GLP-1减肥药,GPCR撑起了现代制药界的半壁江山。
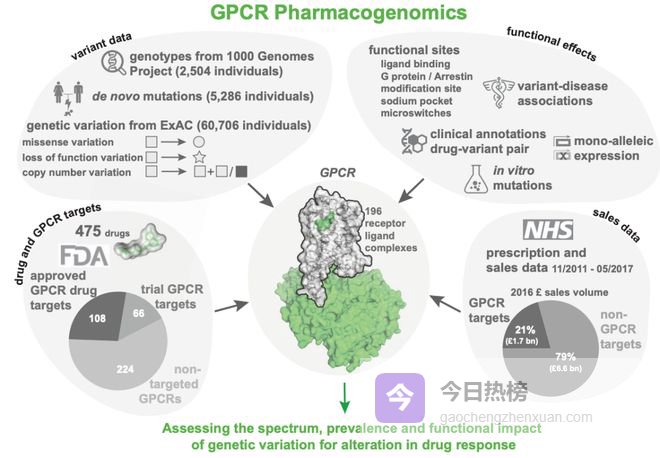
然而GPCR药物的研发正逐渐陷入一场深深危机!
传统的设计中GPCR被全面激活,同时触发多条下游信号通路。
结果疗效与副作用齐飞,患者在获得治疗益处同时不得不忍受药物耐受、受体脱敏、胃肠道反应,甚至致命毒副作用。
如何打破这种伤敌一千,自损八百的困局?
近年随着结构生物学的突破和AI计算化学的深度赋能,一个颠覆性概念正从实验室走向临床:偏向性信号传导(Biased Signaling)。
Part 01

激活与抑制的博弈

新一代偏向性配体不再是简单开关,而极其精密的诱导并稳定受体的特定三维构象,选择性地启动治疗通路,同时关闭引发副作用的有害通路。
这不仅是药理学的底层革命,更是解锁剩余60%未开发GPCR靶点、重塑生物医药千亿赛道的终极密码。
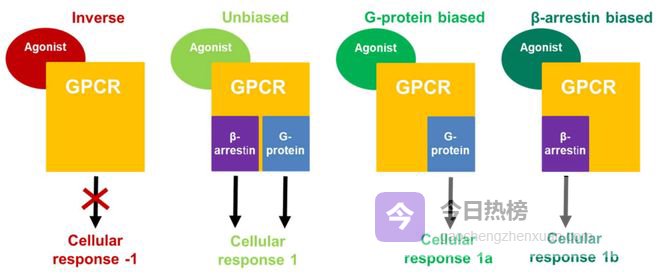
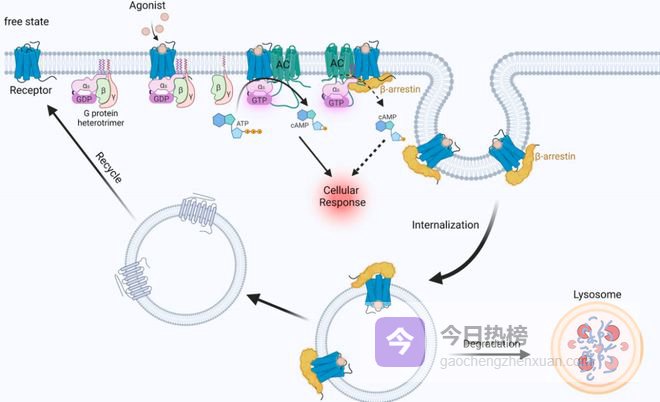
经典GPCR信号中,受体激活后会招募两大类胞内效应蛋白,G蛋白和β-Arretin蛋白。
G蛋白通路被认为介导主要生理功能和疗效的有益通路;
β-Arretin通路负责受体脱敏(让受体失去反应能力)、受体内化通路,与药物副作用、耐药性直接相关。
在传统药物眼中,这两条通路是绑定的套餐,想要G蛋白疗效,就必须咽下β-Arretin带来的副作用。
然而,偏向性激动剂打破了这一规律,通过改变配体结构,结合到GPCR后只激活G蛋白通路(G蛋白偏向),或只激活β-Arrestin通路(Arrestin偏向)。
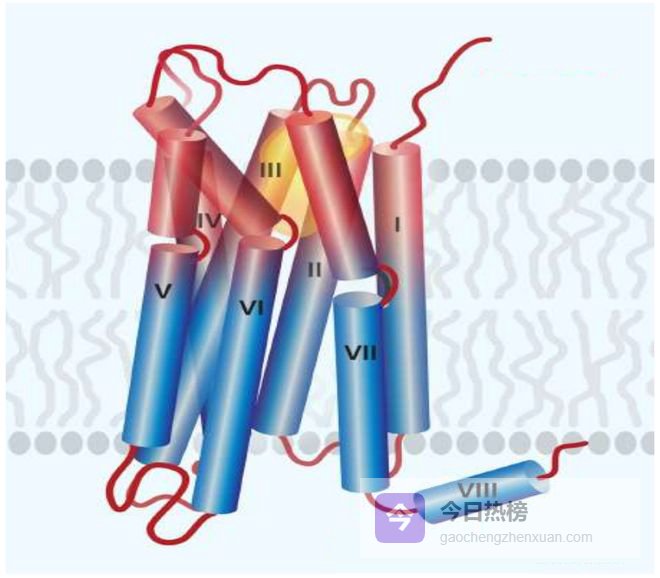
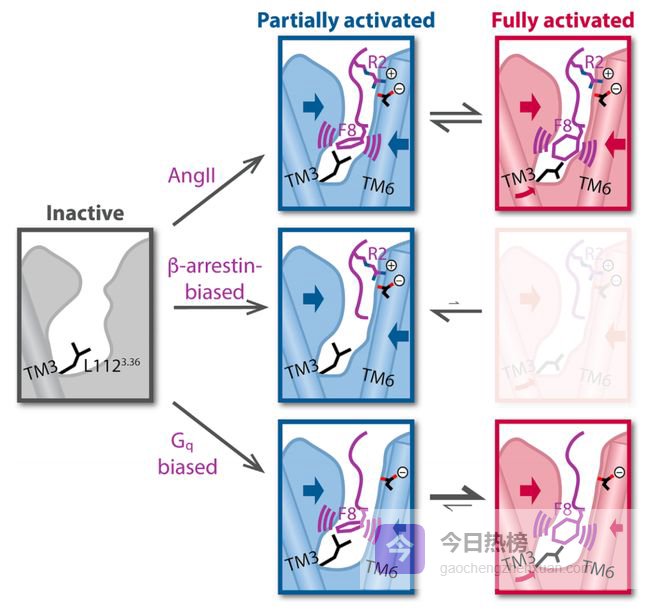
偏向性并非某种玄学魔法,而是源于微观物理结构的精准契合。
在原子分辨率下可看到当偏向性配体进入GPCR结合口袋时,其微小的侧链结构差异,会引发受体跨膜螺旋(特别是TM6)发生不同程度扭曲和位移。
这独特构象变化,被偏向性配体锁定并稳定下来,最终这种特定三维形状只与G蛋白契合,而让β-Arrestin无从下口。
Part 02

直击临床痛点

科学突破最终要服务于临床痛点,偏向性药物对准了医药界几大百亿疾病领域的阿喀琉斯之踵,展现出惊叹的治疗潜力。
场景一:中枢神经,终结阿片类药物致命副作用
这是偏向性理论最经典,也最迫切的临床场景。阿片类药物(如吗啡、芬太尼)镇痛已有上百年历史,它们靶向的是大脑中阿片受体。
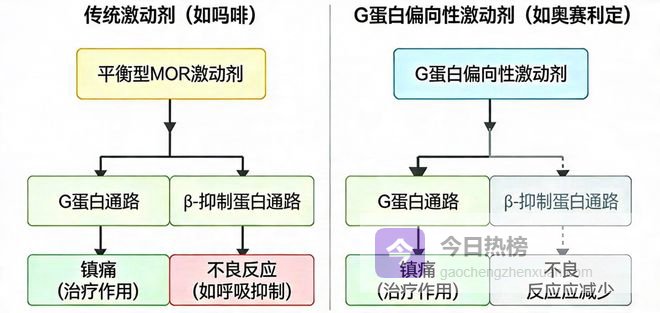
传统阿片类药物在全面激活受体时G蛋白通路带来了强大镇痛效果,但同时激活的β-Arrestin通路却导致严重呼吸抑制(阿片类药物致死的最主要原因)、胃肠道反应及耐药。
阿片类药物引发的危机,已经成为全球公共卫生的巨大灾难。
而偏向性理论为这一百年困局提供了完美解法!
通过设计G蛋白偏向性阿片受体激动剂,药物在提供强效镇痛同时,避开招募β-Arrestin,从而极大拓宽药物安全窗,让安全且强效的镇痛成为可能。
场景二:打破耐药魔咒
在哮喘和慢性阻塞性肺病中,β-肾上腺素受体激动剂是扩张支气管的急救与维持药物。
但患者长期使用后会面临耐药。传统激动剂激活受体后,强烈的β-Arrestin招募促使受体被迅速内吞降解,细胞表面受体数量锐减。
而新型偏向性激动剂则只激活介导支气管扩张的G蛋白通路,完全不引起受体的内化降解敏。这意味着患者长期用药后也能保持稳定、卓越疗效。
场景三:下一代GLP-1破局密钥
受捧的GLP-1减肥神药如司美格鲁肽和替尔泊肽并非完美,严重胃肠道恶心、呕吐,及减重伴随的肌肉流失,是限制依从性和长期应用的最大障碍。
G蛋白偏向性激动剂在体内模型中展现出了比传统非偏向性药物更优的代谢调控和减重效果。
全球顶尖科研团队和Biotech正试图通过偏向性多肽设计,开发只保留降糖减重G蛋白信号、剔除导致恶心呕吐和脱敏通路的下一代GLP-1药物。
谁能在这场去副作用化的偏向性竞赛中胜出,谁就能毫无悬念地拿下下一个千亿美金级别的代谢市场。
Part 03

AI和计算化学,偏向性药物设计引擎

评估GPCR偏向性极其困难,体外细胞测得的偏向性指数很难转化为动物乃至人体真实疗效,这种转化鸿沟让无数药企折戟沉沙!
AI与计算化学的介入,彻底重塑了这一领域的研发范式。
GPCR在细胞膜中是不断变化的动态分子,结构生物学虽然提供了GPCR的高清三维照片,但终究是静态的。
借助强大的AI算力和分子动力学模拟,可以在超级计算机中让整个受体动起来。
在虚拟环境中模拟数百万小分子或多肽与受体结合的动态过程,观察它们如何以毫秒级速度改变跨膜螺旋构象,并精确计算出这种构象招募G蛋白和Arrestin的自由能差异。
过去需要耗费数年时间、合成成千上万个化合物、进行海量体外生化实验才能摸索出的偏向性构效关系,现在通过AI平台几周内就能锁定最优解。
Part 04

领跑者的风采

无论科学故事多么性感,市场看到都是转化价值!
放眼全球产业版图,一批极具远见和技术壁垒的先锋企业已在这个赛道跑出身位,并获得资本与跨国药企的重金押注。
提到偏向性药物的商业化,就绕不开美国公司Trevena。
基于诺奖的GPCR理论,Trevena耗时多年开发了Olinvyk,一种靶向阿片受体的、静脉注射用G蛋白偏向性激动剂,用于治疗中重度急性疼痛,并在2020年获FDA批准上市。
临床数据确凿地证明了与等效剂量吗啡比,Olinvyk能显著减少呼吸抑制的发生率,并大幅降低严重恶心和呕吐。
Olinvyk的获批是一个划时代里程碑,向全世界的药企和监管机构证明偏向性信号传导理论是完全可以转化为安全、有效且能通过FDA的上市新药。
在依靠结构生物学的偏向性设计领域,Nxera Pharma(前身为著名GPCR企业Sosei Heptares)无疑是绝对王者。
这家公司拥有一项名为 StaR (Stabilized Receptor)的独家核心技术。
GPCR在提取出胞膜后极不稳定,很难进行结构解析。StaR技术通过引入少量突变,将GPCR冻结在特定构象中(如专属于G蛋白激活的偏向性构象),随后进行高分辨率结构解析和药物筛选。
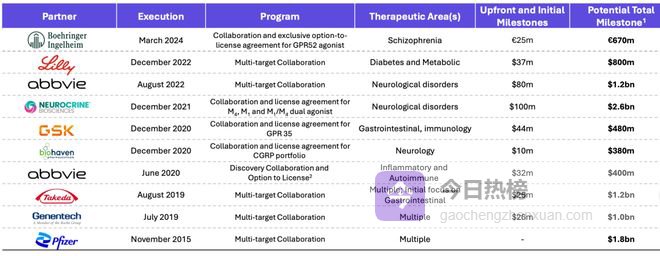
凭借这一壁垒极高的平台,Nxera已经成为全球大药企宠儿,先后与艾伯维、辉瑞、罗氏等巨头达成总价值数十亿美元的合作和管线开发协议。
大药企们真金白银的投入,是对偏向性结构靶向技术最强有力的背书。
最近火热的Structure Therapeutics,作为一家结合计算化学、AI平台与结构生物学的临床阶段Biotech,其核心竞争力正是对复杂GPCR构象的精准控制。
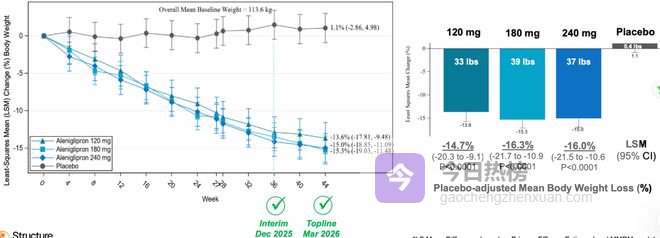
核心管线GSBR-1290瞄准了吸金的代谢赛道小分子GLP-1受体激动剂。硕迪生物依靠基于结构的精准设计平台,在分子层面精心雕琢,力求在口服小分子中复刻甚至超越注射用多肽的完美信号传导轨迹。
其在资本市场受到的热捧,充分展示了GPCR结构控制 代谢大市场所蕴含的惊人爆发力。
Part 05

胖猫的结语

结构生物学揭示精细构象 AI计算化学提供精准筛选 偏向性信号理论指导完美临床转化,这三大前沿技术的历史性合流,构筑了下一代GPCR靶向新药研发的金三角!
属于GPCR的新时代已悄然降临!一个价值数千亿美元的广阔蓝海才刚刚掀开冰山一角!
如果您喜欢胖猫的分析和风格,欢迎扫码加入胖猫的知识星球!获取更多知识、观点以及和胖猫深度链接~

原创文章,作者:马超,如若转载,请注明出处:http://www.gaochengzhenxuan.com/keji/19737.html

